Penemuan Neutron
Pada era 1900-an dipercaya bahwa elektron adalah bagian dari nukleus sama seperti proton. Tetapi, hal ini tidak mungkin terjadi dikarenakan berbagai macam alasan yang diantaranya adalah :
Ukuran dari nukleus yang terlalu kecil bagi elektron. Jika ukuran ini terlalu kecil bagi elektron, sudah pasti ukuran ini juga pasti terlalu kecil untuk proton kan? Tapi bukan ini yang terjadi di partikel pada skala quantum. Berdasarkan hukum ketidakpastian Heisenberg, semakin besar probabilitas sebuah partikel untuk ada di suatu tempat, maka semakin besar juga variasi momentum dari partikel itu. Hal ini berlaku baik untuk elektron maupun proton. Hanya saja perbedaannya adalah elektron memiliki massa yang jauh lebih kecil ketimbang proton. Artinya, nilai momentum yang besar dari elektron berasal dari energi kinetiknya bukan massanya, beda halnya dengan proton. Jadi bisa saja elektron memiliki energi yang sangat besar yang tidak memungkinkan bagi nucleus untuk menahannya dan akhirnya elektron harus dilepaskan.
Spin dari nucleus yang tidak sesuai. Pernyataan ini muncul dari hasil pengamatan deuteron. Nilai spin dari deuteron adalah 1. Jika menggunakan asumsi lama yaitu elektron adalah bagian dari inti atom, itu artinya inti deuteron terdiri dari dua buah proton dan satu buah elektron. Baik proton maupun elektron punya nilai spin yang sama yaitu ½. Itu artinya jika ingin menggunakan asumsi ini, seharusnya deuteron punya nilai spin sebesar 1 ½.
Momentum magnetik dari inti atom. Elektron punya nilai momentum magnetik yang 1000 kali lebih besar ketimbang proton. Itu artinya, nilai momentum magnetik inti atom seharusnya hampir sama dengan momentum magnetik elektron. Tapi, berdasarkan pengamatan yang telah dilakukan, momentum magnetik inti atom justru hampir sama nilainya dengan momentum magnetik proton.
Isi Dari Inti Atom
Inti atom dari sebuah atom terdiri dari beberapa proton dan beberapa neutron. Jumlah dari proton yang ada pada inti atom biasanya sama dengan jumlah elektron yang ada di atom tersebut. Sedangkan jumlah neutron adalah jumlah nomor massa yang dikurangi dengan jumlah proton atau yang biasanya disebut sebagai nomor atom. Lebih lengkapnya dapat dituliskan dengan ilustrasi berikut.
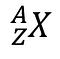

Ada beberapa kombinasi dari inti atom yang ada diantaranya adalah :
Isotop : yaitu inti atom yang memiliki nomor atom Z yang sama. Itu artinya, isotop memiliki jumlah proton yang sama satu dengan yang lainnya.
Isobar : yaitu inti atom yang memiliki nomor massa yang sama. Contohnya adalah ¹⁶C, ¹⁶N, ¹⁶O, dan ¹⁶F.
Isoton : yaitu inti atom yang memiliki jumlah neutron yang sama. Contohnya adalah ¹⁴C , ¹⁵N, ¹⁶O dan ¹⁷F.
Atom terdiri dari inti atom dan elektron. Inti atom tersusun dari proton dan neutron. Masing-masing dari elektron, proton maupun neutron memiliki massa dimana penjumlahan semua massa proton, neutron dan elektron sebanding dengan massa keseluluhan dari atom tersebut (tidak sama tapi sebanding, karena msaih dipengaruhi oleh energi ikat atau binding energy).
Untuk memudahkan analogi, telah disepakati bahwa massa partikel maupun inti atom dituliskan dengan satuan u. Satuan ini memiliki nilai yang sama dengan massa inti atom ¹²C yang dibagi dengan 12. Berdasarkan persamaan Einstein, dapat dipahami juga bahwa massa adalah salah satu bentuk energi, maka satuan massa partikel pun juga bisa dituliskan dengan satuan energi. Satuan yang biasanya digunakan untuk konversi adalah MeV. Konversi dari u ke MeV adalah sebagai berikut.

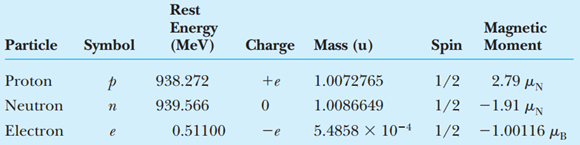
Massa dan spesifikasi dari masing-masing komponen pautoroton, neutron dan elektron adalah sebagai berikut.
![]()
Terdapat 4 jenis gaya mendasar yang ada di alam semesta. Keempat jenis gaya tersebut adalah gaya elektrik, gaya lemah (wak force), gaya kuat (strong force) dan gaya gravitasi. Diantara keempat jenis gaya ini, gaya gravitasi adalah jenis gaya yang paling lemah sedangkan sesuai dengan namanya, gaya kuat adalah gaya yang paling kuat dari keempat jenis gaya yang ada.
Gaya kuat ini juga biasanya dikenal sebagai gaya nuklir (nuclear force). Istilah ini dapat melekat pada gaya kuat karena gaya ini memang adalah gaya nuklir karena skalanya yang sangat kecil. Gaya ini hanya akan bisa terasa jika partikel berada pada jarak yang sangat dekat. Bahkan jika jarak dari dua buah partikel sudah melebihi 10-¹⁴ m, gaya yang paling kuat ini sudah tidak bisa lagi dirasakan efeknya karena telah benar-benar hilang. Inilah alasan mengapa meskipun gaya ini adalah jenis gaya yang paling kuat, gaya ini tetap sulit untuk dideteksi.
Neutron sendiri karena merupakan salah satu jenis nukleon (komponen penyusun inti atom, biasanya istilah yang digunakan untuk menggantikan proton atau neutron), akan merasakan efek dari keberadaan gaya kuat. Tapi tentu, efeknya hanya akan terasa jika neutron berada pada posisi yang dekat dengan inti atom. Selain itu, neutron pun tidak memiliki muatan listrik seperti proton atau pun elektron sehingga tidak akan terpengaruh oleh medan magnet. Jadi neutron adalah partikel yang paling sering digunakan untuk mencari tahu ukuran dari sebuah inti atom. Hal ini dilakukan dengan cara melihat lintasan dari neutron yang ditabrakkan (neutron scattering) ke sejumlah partikel.
Jari-jari dari inti atom bisa diperkirakan dengan persamaan berikut :
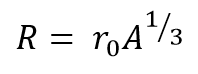 Dimana ro adalah konstanta yang memilki nilai 1.2 x 10–¹⁵ m atau sama dengan 1.2 femtometer.
Dimana ro adalah konstanta yang memilki nilai 1.2 x 10–¹⁵ m atau sama dengan 1.2 femtometer.
Stabilitas
Inti atom yang terdiri dari proton dan neutron tidak selamanya stabil. Yang dimaksud dengan kata stabil disini adalah tidak memiliki kecenderungan yang besar untuk berubah ke bentuk inti atom yang lain. Artinya, beberapa inti atom memiliki kemampuan untuk berubah menjadi jenis inti atom lain.
Perubahan ini tidak terjadi serta merta begitu saja. Ada hal-hal lain yang terjadi ketika inti atom ini berubah menjadi bentuk yang lain. Disinilah biasanya partikel-partikel radiasi dihasilkan. Ada tiga jenis radiasi yang paling umum terjadi yaitu radiasi alpha, radiasi beta, dan radiasi gamma.
Agar inti atom bisa berubah menjadi inti atom lain, inti atom yang baru harus memiliki massa yang lebih kecil dibandingkan inti atom yang lama. Inti atom yang stabil adalah inti atom yang memiliki massa yang paling kecil dari semua jenis isobar yang ada dari inti atom tersebut. Ingat bahwa isobar adalah beberapa jenis inti atom yang memiliki nomor massa yang sama. Jika sebuah inti atom tidak memiliki massa yang cukup kecil, inti atom akan berusaha sebisa mungkin untuk memancarkan radiasi agar bisa mengurangi massa yang dimilikinya.
Sebuah inti atom memiliki kecenderungan untuk memiliki jumlah neutron dan proton yang sama jika nomor massa dari inti atom tersebut kecil. Jika nomor massa dari inti atom tersebut sedang atau bahkan besar, inti atom harus memiliki jumlah neutron yang melebihi jumlah proton. Hal ini dikarenakan neutron tidak memiliki muatan listrik yang memungkinkan adanya gaya tolak menolak. Berbeda halnya dengan proton yang bermuatan dan memiliki gaya tolak menolak satu dengan yang lainnya. Disamping itu, neutron dan proton juga akan memiliki energi ikat (binding energy) yang membuat sebuah inti atom tetap merekat dan utuh. Hanya saja neutron jauh lebih dibutuhkan oleh inti atom berukuran besar karena neutron hanya akan menambah gaya ikat tanpa menambah gaya tolak menolak.
Berdasarkan hasil observasi yang selama ini dilakukan, tidak ada inti atom yang stabil yang memiliki nomor massa lebih dari 209 atau nomor massa lebih dari 83. Biasanya juga, inti atom yang stabil akan memiliki jumlah proton atau jumlah neutron yang genap karena ini akan memudahkan mereka untuk berpasang-pasangan. Hanya ada 4 inti atom stabil yang memiliki proton dan neutron berjumlha ganjil dan semuanya adalah inti atom berukuran kecil. Keempat inti atom ini adalah ²H, ⁶Li, ¹⁰B, dan ¹⁴N. Inti atom yang memiliki nilai energi ikat per nukleon (energi ikat total dibagi nomor massa) yang paling besar adalah ⁵⁶Fe kemudian dilanjutkan oleh beberapa inti-inti atom yang lain yang memiliki nomor massa hampir sama dengan ⁵⁶Fe.
Mengapa alam cenderung lebih suka membuat inti atom yang memiliki jumlah proton dan neutron yang genap? Ini disebabkan sebuah teori yang disebut sebagai prinsip eksklusi Pauli (Pauli exclusion principle). Berdasarkan teori ini, semua partikel-partikel yang berukuran kecil baik itu proton, neutron atau elektron ayng perilakunya hanya bisa dijelaskan dengan konsep mekanika kuantum tidak mungkin memiliki keadaan kuantum yang sama. Partikel-partikel yang berukuran kecil ini tidak berperilaku layaknya benda yang berukuran besar dimana kita bisa memastikan dimana posisi dari benda tersebut. Partikel berukuran kecil tidak memiliki kepastian mengenai letak posisinya, begitu juga mengenai keadaan-keadaan lainnya seperti kecepatan. Tidak ada kepastian hanya ada probabilitas. Probabilitas ini biasanya dijelaskan menggunakan persamaan gelombang. Partikel-partikel ini memiliki kesempatan yang kecil untuk memiliki persamaan gelombang posisi yang sama. Jika sampai ada partikel yang persamaan gelombang yang sama, itu artinya ada kemungkinan partikel-partikel tersebut berada pada posisi yang sama, dimana hal ini tidak memungkinkan untuk terjadi berdasarkan prinsip Pauli. Sehingga, partikel-partikel ini harus memiliki spin yang berbeda. Sedangkan, baik proton dan neutron memiliki nilai spin yang sama yaitu ± ½ . Hanya ada dua kemungkinan, positif atau negatif.
Jadi jika diibaratkan inti atom itu adalah hotel yang tersusun dari banyak kamar, kamar-kamar ini hanya boleh diisi oleh dua orang, tidak kurang atau tidak lebih karena jika sampai kurang dari dua orang, orang yang sendirian ini akan merasa kesepian dan mencari tempat lain agar tidak menjadi sendiri lagi. Jika sampai diisi lebih dari dua orang maka akan membuat ketidaknyamanan yang mengakibatkan ruangna tersebut tidak stabil.
Gejala stabilitas dari inti atom ini biasa dijelaskan dengan menggunakan grafik stabilitas. Dapat dilihat bahwa garis stabilitas (line of stability) menunjukkan bahwa inti atom cenderung lebih stabil ketika inti atom tersusun oleh proton dan neutron dengan jumlah yang sama ketika jumlah proton dari inti atom sedikit. Ketika jumlah proton bertambah banyak, garis stabilitas terlihat semakin naik yang menunjukkan dibutuhkan lebih banyak neutron di dalam inti atom untuk bisa menjadi lebih stabil.
 Garis kestabilan (line of stablity)
Garis kestabilan (line of stablity)
 Energi ikat (binding energy) per nukleon
Energi ikat (binding energy) per nukleon
Inti-inti atom yang tidak stabil, akan berusaha sebisa mungkin untuk berubah menjadi stabil. Hal ini dilakukan dengan cara melakukan peluluhan (decaying) yang bisa dituliskan dengna sebuah persamaan matematika berikut.
 Dimana N0 adalah jumlah partikel atau satuan apapun yang menggambarkan perbandingan jumlah partikel pada kondisi awal. Kemudian λ adalah konstanta peluluhan yang berbeda-beda bagi setiap inti atomnya. Gejala peluluhan ini mengikuti aturan eksponensial.
Dimana N0 adalah jumlah partikel atau satuan apapun yang menggambarkan perbandingan jumlah partikel pada kondisi awal. Kemudian λ adalah konstanta peluluhan yang berbeda-beda bagi setiap inti atomnya. Gejala peluluhan ini mengikuti aturan eksponensial.
Dari persamaan ini jugalah didapatkan sebuah konstanta baru yang sebenarnya lebih sering digunakan ketimbang λ yaitu waktu-paro (half-life). Sama halnya dengan λ yang nilainya berbeda-beda untuk setiap inti atom, waktu-paro pun juga nilainya berbeda-beda untuk masing-masing inti atom yang berbeda. Dari persamaan peluluhan eksponensial bisa didapatkan nilai dari waktu-paro yaitu sebesar 0.693/ λ.
Peluluhan Radioaktif
Dari penjelasan yang sudah diberikan diatas dapat dipahami bahwa inti atom yang tidak stabil akan berusaha sebisa mungkin untuk berubah menjadi inti atom baru yang lebih stabil. Perubahan ini biasanya dikenal sebagai peluluhan (decaying) yaitu ketika inti atom yang tidak stabil ini berubah menjadi inti atom baru sambil memancarkan partikel radiasi.
Salah satu syarat utama agar peluluhan ini dapat terjadi adalah inti atom yang baru harus memiliki energi ikat per nukleon yang lebih besar. Inti atom yang memiliki energi ikat per nukleon yang lebih besar pasti akan lebih stabil.
Untuk mengetahui apakah energi ikat per nukleon dari inti atom yang baru lebih besar atau lebih kecil biasanya dihitunglah sebuah nilai Q yaitu energi kinetik total untuk inti atom yang baru dan partikel radiasi yang dipancarkannya.
Lalu apa hubungannya energi ikat per nukleon dengan energi kinetik total? Secara tersirat pertanyaan ini cukup sulit utnuk dijawab, tapi persamaan Einstein E=mc² telah membuktikan bahwa dua hal ini berkaitan secara erat. Berdasarkan persamaan ini, bisa dipahami bahwa massa adalah salah satu bentuk energi. Bahkan massa adalah metode yang paling efektif untuk menyimpan energi.
Energi ikat per nukleon adalah massa yang hilang dari inti atom yang digunakan untuk mengikat nukleon-nukleon yang ada agar dapat terbentuk sebuah inti atom. Ingat! Massa yang hilang ini tidak sepenuhnya hilang karena ia hanya berubah wujud menjadi wujud energi yang lain. Ketika sebuah inti atom meluluh, maka akan dihasilkan inti atom baru disertai dengan partikel radiasinya dengan masing-masing energi kinetiknya. Nilai dari energi kinetik total ini atau Q bisa diperoleh dari persamaan berikut.
 Dimana masing-masing dari mp dan mr adalah massa inti atom lama dan inti atom baru. Sedangkan mx adalah massa dari partikel radiasi. Jika partikel radiasi yang dihasilkan adalah gamma γ, maka massa partikel radiasi bisa diabaikan. Ketika sebuah inti atom meluluh, nilai Q pasti bertanda positif. Jika nilai Q negatif, maka peluluhan tidak memungkinkan untuk terjadi sehingga peluluhan tersebut tidak akan terjadi.
Dimana masing-masing dari mp dan mr adalah massa inti atom lama dan inti atom baru. Sedangkan mx adalah massa dari partikel radiasi. Jika partikel radiasi yang dihasilkan adalah gamma γ, maka massa partikel radiasi bisa diabaikan. Ketika sebuah inti atom meluluh, nilai Q pasti bertanda positif. Jika nilai Q negatif, maka peluluhan tidak memungkinkan untuk terjadi sehingga peluluhan tersebut tidak akan terjadi.
Peluluhan Alpha
Diantara peluluhan-peluluhan yang paling umum untuk terjadi adalah peluluhan alpha, beta dan gamma. Itu artinya alpha merupkan salah satu jenis peluluhan radioaktif yang cukup sering terjadi. Tetapi, berbeda dengan jenis peluluhan beta dan gamma, jenis peluluhan alpha akan menghasilkan dua buah inti atom baru yang berukuran besar. Hal ini jelas-jelas berbeda dengan peluluhan beta dan gamma yang hanya menghasilkan partikel-partikel dengan massa yang kecil, bahkan untuk gamma hampir tidak memiliki massa sama sekali disertai inti atom baru yang massanya hampir sama dengan inti atom produk atau inti atom yang lama.
Di saat peluluhan alpha terjadi, inti atom yang meluluh membelah diri menjadi dua buah inti atom baru yang dimana salah satunya adalah inti atom helium yang terdiri dari dua buah proton dan dua buah neutron. Dua buah proton dan dua buah neutron ini tidak serta merta terbentuk dan bergabung begitu saja di dalam inti atom. Beberapa teori menyatakan bahwa nukleon yang berada di dalam inti atom memiliki kemampuan dan kebebasan untuk bergerak di dalam sebuah area tertentu. Area ini yang disebut sebagai jari-jari inti atom berdasarkan teori ini. Jadi proton dan neutron yang menyusun inti atom bergerak bebas dan acak di dalam inti atom.
Karena nukleon-nukleon ini bergerak secara acak di dalam inti atom, maka beberapa proton dan neutron bisa saja bergabung menjadi satu dan membentuk sebuah inti atom helium. Jika inti atom helium ini memiliki energi yang mencukupi, inti atom helium ini memiliki kemungkinan yang besar untuk lepas dan menjadi bebas.
Tetapi tentu saja hal ini tidak selalu terjadi. Alpha atau inti atom helium ini hanya bisa terbentuk jika inti atom yang mengungkung proton-proton dan neutron-neutron ini berukuran cukup besar. Inilah alasan mengapa radiasi alpha biasanya terjadi di dalam inti atom yang memiliki nomor massa yang besar, karena dengan nomor massa yang besar inti atom akan memiliki ukuran jari-jari yang besar juga.
Selain itu, batas energi yang sebenarnya harus dimiliki partikel alpha untuk terlepas dari inti atom adalah sebesar 20 MeV. Energi sebesar ini tidak mungkin dimiliki oleh sebuah partikel alpha secara alami. Pada umumnya, ketika partikel alpha terlepas dari inti atom dan terpancar sebagai radiasi, partikel alpha hanya memiliki energi rata-rata sebesar 6 MeV.
Tetapi partikel alpha tetap bisa terlepas dari inti atom dikarenakan fenomena mekanika kuantum yang dikenal sebagai quantum tunneling. Fenomena quantum tunneling terjadi ketika sebuah partikel bisa melewati sebuah pembatas secara cuma-cuma tanpa bereaksi apapun. Kejadian semacam ini tidak mungkin terjadi di dunia makro, dunia yang selama ini kita rasakan. Quantum tunneling hanya memungkinkan untuk terjadi pada partikel berukuran kecil yang berperilaku berdasarkan prinsip mekanika kuantum. Dengan prinsip quantum tunneling ini, memungkinkan bagi partikel alpha untuk terlepas meskipun sebenarnya partikel ini tidak punya energi yang cukup untuk terlepas.
Seperti yang telah dibahas diatas, salah satu syarat utama inti atom dapat meluluh menjadi inti atom yang lebih stabil adalah nilai Q dari persamaan peluluhan bernilai positif. Maka dari semua kemungkiann peluluhan yang ada bagi sebuah inti atom yang tidak stabil perlu dicek satu per satu apakah Q bernilai positif atau tidak.
Peluluhan Beta
Ada berbagai macam alasan mengapa sebuah inti atom menjadi tidak stabil. Salah satu diantaranya adalah karena terdapat neutron yang menyebabkan inti atom ini tidak stabil. Neutron ini bisa saja menyebabkan ketidakstabilan karena tidak berpasangan atau inti atom memang sudah mengandung terlalu banyak neutron. Untuk itu, neutron ini pun harus dihilangkan bagaimanapun caranya.
Neutron ini bisa hilang dengan cara mengubahnya menjadi bentuk lain. Bentuk perubahan yang paling banyak diusulkan adalah perubahan menjadi proton dan elektron. Usulan tersebut dapat dituliskan dengan persamaan.
 Tetapi perubahan ini mengandung beberapa keanehan tersendiri. Salah satu hal yang membuat persamaan ini menjadi aneh adalah perubahan nilai spin. Neutron memiliki niali spin sebesar ± ½. Begitu pun juga dengan proton dan neutron. Itu artinya, tidak ada keseimbangan nilai spin pada persamaan tersebut. Pada sisi kiri persamaan nilai total spin adalah ± ½, tetapi di sebelah kanan nilai total spin
Tetapi perubahan ini mengandung beberapa keanehan tersendiri. Salah satu hal yang membuat persamaan ini menjadi aneh adalah perubahan nilai spin. Neutron memiliki niali spin sebesar ± ½. Begitu pun juga dengan proton dan neutron. Itu artinya, tidak ada keseimbangan nilai spin pada persamaan tersebut. Pada sisi kiri persamaan nilai total spin adalah ± ½, tetapi di sebelah kanan nilai total spin

Terdapat 4 jenis gaya mendasar yang ada di alam semesta. Keempat jenis gaya tersebut adalah gaya elektrik, gaya lemah (wak force), gaya kuat (strong force) dan gaya gravitasi. Diantara keempat jenis gaya ini, gaya gravitasi adalah jenis gaya yang paling lemah sedangkan sesuai dengan namanya, gaya kuat adalah gaya yang paling kuat dari keempat jenis gaya yang ada.
Gaya kuat ini juga biasanya dikenal sebagai gaya nuklir (nuclear force). Istilah ini dapat melekat pada gaya kuat karena gaya ini memang adalah gaya nuklir karena skalanya yang sangat kecil. Gaya ini hanya akan bisa terasa jika partikel berada pada jarak yang sangat dekat. Bahkan jika jarak dari dua buah partikel sudah melebihi 10-¹⁴ m, gaya yang paling kuat ini sudah tidak bisa lagi dirasakan efeknya karena telah benar-benar hilang. Inilah alasan mengapa meskipun gaya ini adalah jenis gaya yang paling kuat, gaya ini tetap sulit untuk dideteksi.
Neutron sendiri karena merupakan salah satu jenis nukleon (komponen penyusun inti atom, biasanya istilah yang digunakan untuk menggantikan proton atau neutron), akan merasakan efek dari keberadaan gaya kuat. Tapi tentu, efeknya hanya akan terasa jika neutron berada pada posisi yang dekat dengan inti atom. Selain itu, neutron pun tidak memiliki muatan listrik seperti proton atau pun elektron sehingga tidak akan terpengaruh oleh medan magnet. Jadi neutron adalah partikel yang paling sering digunakan untuk mencari tahu ukuran dari sebuah inti atom. Hal ini dilakukan dengan cara melihat lintasan dari neutron yang ditabrakkan (neutron scattering) ke sejumlah partikel.
Jari-jari dari inti atom bisa diperkirakan dengan persamaan berikut :
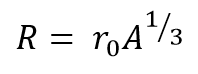
Stabilitas
Inti atom yang terdiri dari proton dan neutron tidak selamanya stabil. Yang dimaksud dengan kata stabil disini adalah tidak memiliki kecenderungan yang besar untuk berubah ke bentuk inti atom yang lain. Artinya, beberapa inti atom memiliki kemampuan untuk berubah menjadi jenis inti atom lain.
Perubahan ini tidak terjadi serta merta begitu saja. Ada hal-hal lain yang terjadi ketika inti atom ini berubah menjadi bentuk yang lain. Disinilah biasanya partikel-partikel radiasi dihasilkan. Ada tiga jenis radiasi yang paling umum terjadi yaitu radiasi alpha, radiasi beta, dan radiasi gamma.
Agar inti atom bisa berubah menjadi inti atom lain, inti atom yang baru harus memiliki massa yang lebih kecil dibandingkan inti atom yang lama. Inti atom yang stabil adalah inti atom yang memiliki massa yang paling kecil dari semua jenis isobar yang ada dari inti atom tersebut. Ingat bahwa isobar adalah beberapa jenis inti atom yang memiliki nomor massa yang sama. Jika sebuah inti atom tidak memiliki massa yang cukup kecil, inti atom akan berusaha sebisa mungkin untuk memancarkan radiasi agar bisa mengurangi massa yang dimilikinya.
Sebuah inti atom memiliki kecenderungan untuk memiliki jumlah neutron dan proton yang sama jika nomor massa dari inti atom tersebut kecil. Jika nomor massa dari inti atom tersebut sedang atau bahkan besar, inti atom harus memiliki jumlah neutron yang melebihi jumlah proton. Hal ini dikarenakan neutron tidak memiliki muatan listrik yang memungkinkan adanya gaya tolak menolak. Berbeda halnya dengan proton yang bermuatan dan memiliki gaya tolak menolak satu dengan yang lainnya. Disamping itu, neutron dan proton juga akan memiliki energi ikat (binding energy) yang membuat sebuah inti atom tetap merekat dan utuh. Hanya saja neutron jauh lebih dibutuhkan oleh inti atom berukuran besar karena neutron hanya akan menambah gaya ikat tanpa menambah gaya tolak menolak.
Berdasarkan hasil observasi yang selama ini dilakukan, tidak ada inti atom yang stabil yang memiliki nomor massa lebih dari 209 atau nomor massa lebih dari 83. Biasanya juga, inti atom yang stabil akan memiliki jumlah proton atau jumlah neutron yang genap karena ini akan memudahkan mereka untuk berpasang-pasangan. Hanya ada 4 inti atom stabil yang memiliki proton dan neutron berjumlha ganjil dan semuanya adalah inti atom berukuran kecil. Keempat inti atom ini adalah ²H, ⁶Li, ¹⁰B, dan ¹⁴N. Inti atom yang memiliki nilai energi ikat per nukleon (energi ikat total dibagi nomor massa) yang paling besar adalah ⁵⁶Fe kemudian dilanjutkan oleh beberapa inti-inti atom yang lain yang memiliki nomor massa hampir sama dengan ⁵⁶Fe.
Mengapa alam cenderung lebih suka membuat inti atom yang memiliki jumlah proton dan neutron yang genap? Ini disebabkan sebuah teori yang disebut sebagai prinsip eksklusi Pauli (Pauli exclusion principle). Berdasarkan teori ini, semua partikel-partikel yang berukuran kecil baik itu proton, neutron atau elektron ayng perilakunya hanya bisa dijelaskan dengan konsep mekanika kuantum tidak mungkin memiliki keadaan kuantum yang sama. Partikel-partikel yang berukuran kecil ini tidak berperilaku layaknya benda yang berukuran besar dimana kita bisa memastikan dimana posisi dari benda tersebut. Partikel berukuran kecil tidak memiliki kepastian mengenai letak posisinya, begitu juga mengenai keadaan-keadaan lainnya seperti kecepatan. Tidak ada kepastian hanya ada probabilitas. Probabilitas ini biasanya dijelaskan menggunakan persamaan gelombang. Partikel-partikel ini memiliki kesempatan yang kecil untuk memiliki persamaan gelombang posisi yang sama. Jika sampai ada partikel yang persamaan gelombang yang sama, itu artinya ada kemungkinan partikel-partikel tersebut berada pada posisi yang sama, dimana hal ini tidak memungkinkan untuk terjadi berdasarkan prinsip Pauli. Sehingga, partikel-partikel ini harus memiliki spin yang berbeda. Sedangkan, baik proton dan neutron memiliki nilai spin yang sama yaitu ± ½ . Hanya ada dua kemungkinan, positif atau negatif.
Jadi jika diibaratkan inti atom itu adalah hotel yang tersusun dari banyak kamar, kamar-kamar ini hanya boleh diisi oleh dua orang, tidak kurang atau tidak lebih karena jika sampai kurang dari dua orang, orang yang sendirian ini akan merasa kesepian dan mencari tempat lain agar tidak menjadi sendiri lagi. Jika sampai diisi lebih dari dua orang maka akan membuat ketidaknyamanan yang mengakibatkan ruangna tersebut tidak stabil.
Gejala stabilitas dari inti atom ini biasa dijelaskan dengan menggunakan grafik stabilitas. Dapat dilihat bahwa garis stabilitas (line of stability) menunjukkan bahwa inti atom cenderung lebih stabil ketika inti atom tersusun oleh proton dan neutron dengan jumlah yang sama ketika jumlah proton dari inti atom sedikit. Ketika jumlah proton bertambah banyak, garis stabilitas terlihat semakin naik yang menunjukkan dibutuhkan lebih banyak neutron di dalam inti atom untuk bisa menjadi lebih stabil.
 Garis kestabilan (line of stablity)
Garis kestabilan (line of stablity) Energi ikat (binding energy) per nukleon
Energi ikat (binding energy) per nukleonInti-inti atom yang tidak stabil, akan berusaha sebisa mungkin untuk berubah menjadi stabil. Hal ini dilakukan dengan cara melakukan peluluhan (decaying) yang bisa dituliskan dengna sebuah persamaan matematika berikut.

Dari persamaan ini jugalah didapatkan sebuah konstanta baru yang sebenarnya lebih sering digunakan ketimbang λ yaitu waktu-paro (half-life). Sama halnya dengan λ yang nilainya berbeda-beda untuk setiap inti atom, waktu-paro pun juga nilainya berbeda-beda untuk masing-masing inti atom yang berbeda. Dari persamaan peluluhan eksponensial bisa didapatkan nilai dari waktu-paro yaitu sebesar 0.693/ λ.
Peluluhan Radioaktif
Dari penjelasan yang sudah diberikan diatas dapat dipahami bahwa inti atom yang tidak stabil akan berusaha sebisa mungkin untuk berubah menjadi inti atom baru yang lebih stabil. Perubahan ini biasanya dikenal sebagai peluluhan (decaying) yaitu ketika inti atom yang tidak stabil ini berubah menjadi inti atom baru sambil memancarkan partikel radiasi.
Salah satu syarat utama agar peluluhan ini dapat terjadi adalah inti atom yang baru harus memiliki energi ikat per nukleon yang lebih besar. Inti atom yang memiliki energi ikat per nukleon yang lebih besar pasti akan lebih stabil.
Untuk mengetahui apakah energi ikat per nukleon dari inti atom yang baru lebih besar atau lebih kecil biasanya dihitunglah sebuah nilai Q yaitu energi kinetik total untuk inti atom yang baru dan partikel radiasi yang dipancarkannya.
Lalu apa hubungannya energi ikat per nukleon dengan energi kinetik total? Secara tersirat pertanyaan ini cukup sulit utnuk dijawab, tapi persamaan Einstein E=mc² telah membuktikan bahwa dua hal ini berkaitan secara erat. Berdasarkan persamaan ini, bisa dipahami bahwa massa adalah salah satu bentuk energi. Bahkan massa adalah metode yang paling efektif untuk menyimpan energi.
Energi ikat per nukleon adalah massa yang hilang dari inti atom yang digunakan untuk mengikat nukleon-nukleon yang ada agar dapat terbentuk sebuah inti atom. Ingat! Massa yang hilang ini tidak sepenuhnya hilang karena ia hanya berubah wujud menjadi wujud energi yang lain. Ketika sebuah inti atom meluluh, maka akan dihasilkan inti atom baru disertai dengan partikel radiasinya dengan masing-masing energi kinetiknya. Nilai dari energi kinetik total ini atau Q bisa diperoleh dari persamaan berikut.

Peluluhan Alpha
Diantara peluluhan-peluluhan yang paling umum untuk terjadi adalah peluluhan alpha, beta dan gamma. Itu artinya alpha merupkan salah satu jenis peluluhan radioaktif yang cukup sering terjadi. Tetapi, berbeda dengan jenis peluluhan beta dan gamma, jenis peluluhan alpha akan menghasilkan dua buah inti atom baru yang berukuran besar. Hal ini jelas-jelas berbeda dengan peluluhan beta dan gamma yang hanya menghasilkan partikel-partikel dengan massa yang kecil, bahkan untuk gamma hampir tidak memiliki massa sama sekali disertai inti atom baru yang massanya hampir sama dengan inti atom produk atau inti atom yang lama.
Di saat peluluhan alpha terjadi, inti atom yang meluluh membelah diri menjadi dua buah inti atom baru yang dimana salah satunya adalah inti atom helium yang terdiri dari dua buah proton dan dua buah neutron. Dua buah proton dan dua buah neutron ini tidak serta merta terbentuk dan bergabung begitu saja di dalam inti atom. Beberapa teori menyatakan bahwa nukleon yang berada di dalam inti atom memiliki kemampuan dan kebebasan untuk bergerak di dalam sebuah area tertentu. Area ini yang disebut sebagai jari-jari inti atom berdasarkan teori ini. Jadi proton dan neutron yang menyusun inti atom bergerak bebas dan acak di dalam inti atom.
Karena nukleon-nukleon ini bergerak secara acak di dalam inti atom, maka beberapa proton dan neutron bisa saja bergabung menjadi satu dan membentuk sebuah inti atom helium. Jika inti atom helium ini memiliki energi yang mencukupi, inti atom helium ini memiliki kemungkinan yang besar untuk lepas dan menjadi bebas.
Tetapi tentu saja hal ini tidak selalu terjadi. Alpha atau inti atom helium ini hanya bisa terbentuk jika inti atom yang mengungkung proton-proton dan neutron-neutron ini berukuran cukup besar. Inilah alasan mengapa radiasi alpha biasanya terjadi di dalam inti atom yang memiliki nomor massa yang besar, karena dengan nomor massa yang besar inti atom akan memiliki ukuran jari-jari yang besar juga.
Selain itu, batas energi yang sebenarnya harus dimiliki partikel alpha untuk terlepas dari inti atom adalah sebesar 20 MeV. Energi sebesar ini tidak mungkin dimiliki oleh sebuah partikel alpha secara alami. Pada umumnya, ketika partikel alpha terlepas dari inti atom dan terpancar sebagai radiasi, partikel alpha hanya memiliki energi rata-rata sebesar 6 MeV.
Tetapi partikel alpha tetap bisa terlepas dari inti atom dikarenakan fenomena mekanika kuantum yang dikenal sebagai quantum tunneling. Fenomena quantum tunneling terjadi ketika sebuah partikel bisa melewati sebuah pembatas secara cuma-cuma tanpa bereaksi apapun. Kejadian semacam ini tidak mungkin terjadi di dunia makro, dunia yang selama ini kita rasakan. Quantum tunneling hanya memungkinkan untuk terjadi pada partikel berukuran kecil yang berperilaku berdasarkan prinsip mekanika kuantum. Dengan prinsip quantum tunneling ini, memungkinkan bagi partikel alpha untuk terlepas meskipun sebenarnya partikel ini tidak punya energi yang cukup untuk terlepas.
Seperti yang telah dibahas diatas, salah satu syarat utama inti atom dapat meluluh menjadi inti atom yang lebih stabil adalah nilai Q dari persamaan peluluhan bernilai positif. Maka dari semua kemungkiann peluluhan yang ada bagi sebuah inti atom yang tidak stabil perlu dicek satu per satu apakah Q bernilai positif atau tidak.
Peluluhan Beta
Ada berbagai macam alasan mengapa sebuah inti atom menjadi tidak stabil. Salah satu diantaranya adalah karena terdapat neutron yang menyebabkan inti atom ini tidak stabil. Neutron ini bisa saja menyebabkan ketidakstabilan karena tidak berpasangan atau inti atom memang sudah mengandung terlalu banyak neutron. Untuk itu, neutron ini pun harus dihilangkan bagaimanapun caranya.
Neutron ini bisa hilang dengan cara mengubahnya menjadi bentuk lain. Bentuk perubahan yang paling banyak diusulkan adalah perubahan menjadi proton dan elektron. Usulan tersebut dapat dituliskan dengan persamaan.

adalah 0 atau ± 1.
Maka dari itu, diperlukan teori baru untuk memecahkan ke-ambiguan ini. Teori yang pada akhirnya lahir dan memecahkan masalah ini adalah teori mengenai neutrino. Teori ini pertama kali disulkan pada tahun 1930 oleh Wolfgang Pauli. Jadi terdapat kekurangan pada persamaan reaksi diatas karena tidak mengandung partikel neutrino. Partikel inilah yang memecahkan permasalahan spin pada persaman diatas karena sama halnya dengan proton, neutron atau pun elektron, neutrino juga memiliki nilai spin sebesar ± ½. Sehingga keseimbangan spin dapat dipertahankan, karena baik di sisi kanan (produk) atau pun kiri (reaktan), nilai spin-nya adalah sebesar ± ½.
Selain itu, neutrino jgua memecahkan masalah lain dari teori peluluhan beta. Nilai Q dari reaksi peluluhan sudah seharusnya semua berubah menjadi energi kinetik partikel beta. Tetapi hal ini tidak terjadi. Dengan keberadaan neutrino, keadaan ini bisa dijelaskan. Neutrino membawa sebagian energi Q yang dihasilkan dari proses peluluhan.
 Gambar diatas adalah grafik yang menjelaskan intensitas relative dari elektron atau partikel beta berdasarkan energinya. Q dari persaman peluluhan senilai degnan Kmax pada persamaan tersebut. Itu artinya, nilai Q terbagi menjadi dua dimana satu bagian dibawa oleh partikel beta dan satu bagian lagi dibawa oleh neutrino.
Gambar diatas adalah grafik yang menjelaskan intensitas relative dari elektron atau partikel beta berdasarkan energinya. Q dari persaman peluluhan senilai degnan Kmax pada persamaan tersebut. Itu artinya, nilai Q terbagi menjadi dua dimana satu bagian dibawa oleh partikel beta dan satu bagian lagi dibawa oleh neutrino.
Neutrino adalah salah satu bagian dari standar model dalam fisika partikel (standard model of particle physics), sama dengan elektron dan gamma. Perbedaannya adalah, neutrino sangat sulit bereaksi dengan partikel lain, tidak seperti elektron atau pun gamma.
Elektron dan gamma adalah dua partikel yang dapat bereaksi dengan energi listrik (electric force) atau pun energi kuat (strong force). Sedangkan neutrino tidak memiliki kemampuan itu, dan hanya mau bereaksi dengan perantara energi lemah (weak force). Selebihnya mengenai fisika partikel dan standar model akan dibahas pada artikel lain.
Peluluhan β-
Peluluhan jenis ini adalah peluluhan yang menghasilkan elektron dari dalam inti atom akibat perubahan neutron menjadi proton. Karena elektron ini datangnya dari dalam inti atom, maka dibutuhkan nama baru selain elektron (masa sih pakai nama elektron lagi). Akhirnya nama β- adalah nama yang digunakan untuk menamakan jenis elektron ini.
Kita juga sudah tahu bahwa neutrino adalah bagian dari standar model sama halnya dengan elektron dan gamma atau lebih tepatnya adalah fermion. Fermion adalah jenis partikel yang tidak membawa dan mengandung energi tetapi akan sensitif dan bereaksi terhadap keberadaan energi, bergantung pada jenis fermion tersebut. Contoh, elektron adalah salah satu jenis fermion yang sensitif terhadap keberadaan energi elektromagnet sedangkan neutrino tidak. Di sisi lain, selain ada fermion ada juga boson yaitu partikel yang mengandung energi di dalamnya seperti γ (gamma) yang mengandung energi elektromagnetik.
Masing-masing dari fermion memiliki anti partikelnya sendiri-sendiri. Perbedaan antara partikel dengan anti-partikel hanya pada muatannya saja. Nilai muatan dari sebuah anti-partikel adalah sama dengan negatif dari muatan partikelnya. Contohnya adalah elektron yang bermuatan -1 sedangkan positron atau anti-elektron, anti-partikel dari elektron bermuatan +1. Begitu juga halnya dengan neutrino dan anti-neutrino serta fermion-fermion lain.
Pada peluluhan β-, partikel sampingan yang dihasilkan adalah anti-neutrino. Berikut adalah salah satu
Maka dari itu, diperlukan teori baru untuk memecahkan ke-ambiguan ini. Teori yang pada akhirnya lahir dan memecahkan masalah ini adalah teori mengenai neutrino. Teori ini pertama kali disulkan pada tahun 1930 oleh Wolfgang Pauli. Jadi terdapat kekurangan pada persamaan reaksi diatas karena tidak mengandung partikel neutrino. Partikel inilah yang memecahkan permasalahan spin pada persaman diatas karena sama halnya dengan proton, neutron atau pun elektron, neutrino juga memiliki nilai spin sebesar ± ½. Sehingga keseimbangan spin dapat dipertahankan, karena baik di sisi kanan (produk) atau pun kiri (reaktan), nilai spin-nya adalah sebesar ± ½.
Selain itu, neutrino jgua memecahkan masalah lain dari teori peluluhan beta. Nilai Q dari reaksi peluluhan sudah seharusnya semua berubah menjadi energi kinetik partikel beta. Tetapi hal ini tidak terjadi. Dengan keberadaan neutrino, keadaan ini bisa dijelaskan. Neutrino membawa sebagian energi Q yang dihasilkan dari proses peluluhan.

Neutrino adalah salah satu bagian dari standar model dalam fisika partikel (standard model of particle physics), sama dengan elektron dan gamma. Perbedaannya adalah, neutrino sangat sulit bereaksi dengan partikel lain, tidak seperti elektron atau pun gamma.
Elektron dan gamma adalah dua partikel yang dapat bereaksi dengan energi listrik (electric force) atau pun energi kuat (strong force). Sedangkan neutrino tidak memiliki kemampuan itu, dan hanya mau bereaksi dengan perantara energi lemah (weak force). Selebihnya mengenai fisika partikel dan standar model akan dibahas pada artikel lain.
Peluluhan β-
Peluluhan jenis ini adalah peluluhan yang menghasilkan elektron dari dalam inti atom akibat perubahan neutron menjadi proton. Karena elektron ini datangnya dari dalam inti atom, maka dibutuhkan nama baru selain elektron (masa sih pakai nama elektron lagi). Akhirnya nama β- adalah nama yang digunakan untuk menamakan jenis elektron ini.
Kita juga sudah tahu bahwa neutrino adalah bagian dari standar model sama halnya dengan elektron dan gamma atau lebih tepatnya adalah fermion. Fermion adalah jenis partikel yang tidak membawa dan mengandung energi tetapi akan sensitif dan bereaksi terhadap keberadaan energi, bergantung pada jenis fermion tersebut. Contoh, elektron adalah salah satu jenis fermion yang sensitif terhadap keberadaan energi elektromagnet sedangkan neutrino tidak. Di sisi lain, selain ada fermion ada juga boson yaitu partikel yang mengandung energi di dalamnya seperti γ (gamma) yang mengandung energi elektromagnetik.
Masing-masing dari fermion memiliki anti partikelnya sendiri-sendiri. Perbedaan antara partikel dengan anti-partikel hanya pada muatannya saja. Nilai muatan dari sebuah anti-partikel adalah sama dengan negatif dari muatan partikelnya. Contohnya adalah elektron yang bermuatan -1 sedangkan positron atau anti-elektron, anti-partikel dari elektron bermuatan +1. Begitu juga halnya dengan neutrino dan anti-neutrino serta fermion-fermion lain.
Pada peluluhan β-, partikel sampingan yang dihasilkan adalah anti-neutrino. Berikut adalah salah satu
contoh peluluhan β- dari ¹⁴C.

Peluluhan β+
Sama halnya dengan peluluhan β-, peluluhan β+ jug amenghasilkan partikel sampingan yaitu neutrino. Salah satu contoh peluluhan β+ adalah peluluhan yang terjadi pada ¹⁴O berdasarkan persamaan berikut.
 Penangkapan Elektron (Electron Capturing)
Penangkapan Elektron (Electron Capturing)
Bukan hanya peluluhan β+ dan β- saja yang dapat menghasilkan produk sanmpingan berupa neutrino atau anti-neutrino. Ada juga reaksi yang dikenal sebagai electron capturing atau penangkapan elektron yang juga akan menghasilkan neutrino. Sama juga dengan peluluhan beta, neutrino nantinya akan membawa sebagian energi yang dihasilkan dari proses peluluhan.
Secara sederhana sebuah atom terdiri dari dua buah bagian utama, inti atom dan elektron. Elektron yang terdapat pada sebuah atom akan mengitari inti atom layaknya bumi dan planet-planet yang mengitari matahari (tentu dengan beberapa pengecualian karena elektron berperilaku berdasarkan hukum mekanika kuantum sedangkan planet-planet berdasarkan hukum mekanika Newton).
Karena elektron-elektron yang bermuatan negatif ini berputar mengitari inti atom yang bermuatan positif, maka akan ada kemungkinan dimana elektron jatuh ke dalam inti atom dna terjadi fenomena penangkapan elektron. Terlebih lagi jika jenis atomnya adalah atom non-logam dimana ada banyak elektron di dalam sebuah atom dan di saat yang bersamaan jari-jarinya berukuran kecil.
Elektron yang dapat jatuh ke dalam inti atom adalah elektron-elektron yang berada pada kulit K atau L, yaitu kulit orbit elektron yang paling dekat dengan inti atom. Reaksi yang terjadi pada proses penangkapan elektron dapat dituliskan sebagai berikut.
 Karena elektron-elektron ini telah jatuh ke dalam inti atom, maka posisinya harus digantikan dan diisi oleh elektron lain. Ketika elektron lain ini berpindah posisi untuk mengisi kekosongan yang ada pada kulit K atau L, maka akan dihasilkan radiasi x-ray. Energi dari x-ray akan berbeda-beda untuk masing-masing jenis atom. Maka dari itulah, pancaran x-ray yang dihasilkan dari proses ini biasanya dikenal sebagai characteristic x-ray karena dapat digunakan utnuk mengetahui jenis atom.
Karena elektron-elektron ini telah jatuh ke dalam inti atom, maka posisinya harus digantikan dan diisi oleh elektron lain. Ketika elektron lain ini berpindah posisi untuk mengisi kekosongan yang ada pada kulit K atau L, maka akan dihasilkan radiasi x-ray. Energi dari x-ray akan berbeda-beda untuk masing-masing jenis atom. Maka dari itulah, pancaran x-ray yang dihasilkan dari proses ini biasanya dikenal sebagai characteristic x-ray karena dapat digunakan utnuk mengetahui jenis atom.
Prosesn ini akan menghasilkan neutrino, sama halnya dengan proses pemancaran radiasi β+ karena kedua proses ini adalah proses yang sama-sama melibatkan perubahan proton.
Peluluhan Gamma
Peluluhan gamma adalah satu-satunya jenis peluluhan yang tidak mengakibatkan perubahan nomor massa maupun nomor atom. Itu artinya, fenomena ini tidak membuat jumlah proton atau pun neutron beertambah seperti pada peluluhan alpha juga tidak mengakibatkan berubahnya proton menjadi neutron atau sebaliknya seperti peluluhan beta.
Peluluhan ini hanya terjadi pada inti atom yang kurang stabil. Biasanya terdapat proton atau neutron yang memiliki energi berlebih sehingga menyebabkan ketidakstabilan. Kondisi ini harus segera diubah yaitu dengan cara melepaskan energi yang berlebihan ini. Energi ini lalu dilepaskan dan dibawa dalam bentuk gelombang elektromagnetik atau foton ber-spektrum γ (gamma).
Reaksi dari peluluhan γ dapat dituliskan sebagai berikut.
 Yang dimaksud dengan X* adalah inti atom yang sedang berada pada kondisi tidak stabil. Energi dari γ berbeda-beda untuk setiap jenis inti atomnya. Maka dari itu, pengukuran energi γ pun juga memiliki aplikasi yagn luas di dalam dunia fisika nuklir dimana salah satunya adalah untuk mengetahui jenis atom, sama seperti characteristic x-ray.
Yang dimaksud dengan X* adalah inti atom yang sedang berada pada kondisi tidak stabil. Energi dari γ berbeda-beda untuk setiap jenis inti atomnya. Maka dari itu, pengukuran energi γ pun juga memiliki aplikasi yagn luas di dalam dunia fisika nuklir dimana salah satunya adalah untuk mengetahui jenis atom, sama seperti characteristic x-ray.
Nuklida Radioaktif
Telah disepakati bersama bahwa semua partikel yang ada di alam semesta ini terbentuk dan bermula dari ledakan besar big bang yang terjadi 13,7 miliar tahun silam. Ketika ledakan ini terjadi, tidak serta merta membuat atom-atom berat langsung terbentuk. Ada proses panjang yang harus dilewati sampai akhirnya alam semesta kita menjadi alam semesta seperti yang kita ketahui sekarang.
Alam semesta hanya bisa menyediakan proton dan neutron bebas yang akhirnya bersatu dan membentuk atom-atom hidrogen, dimana atom-atom hidrogen ini menjadi penyusun utama dari semua jenis bintang. Ketika sebuah bintang sudah terbentuk, terjadilah pembakaran yang memicu terbentuknya nuklida-nuklida lain dengan massa yang lebih besar. Sampai akhirnya bintang sudah tidak mampu melakukan pembakaran lagi dan meledakkan supernovae atau planetary nebulae. Ketika ledakan ini terjadi, terbentuk lagilah nulida-nuklida yang lebih berat yang tidak mungkin dibentuk di dalam sebuah bintang.
Bumi yang kita tinggali sekarang mengandung beberapa unsur yang dibentuk dari semua proses panjang ini. Ada yang mengatakan bahwa semua unsur yang pernah terbentuk di alam semesta pasti bisa ditemukan di Bumi tapi sudah habis meluluh, tetapi ada juga yang mengatakan bahwa Bumi tidak mengandung semua unsur yang ada di alam semesta.
Tetapi ketika kita mempertimbangkan usia bumi saat ini, akan sangat sulit untuk membuktikan bahwa semua unsur pernah ada di Bumi. Usia Bumi dan Matahari bisa diperkirakan sama, yaitu sekitar 4,5 miliar tahun (sepertiga dari usia alam semesta). Dari jangka waktu yang selama ini, akan ada besar kemungkinan terdapat radionuklida yang telah meluluh total sehingga tidak mungkin ditemukan saat ini. Dari pengamatan dan penelitian yang telah dilakukan, tidak mungkin ada radionuklida di Bumi yang lebih berat dari 238U, kecuali jika radionuklida ini adalah radionuklida hasil proses buatan manusia. Salah satu radionuklida yang memiliki waktu-paro paling panjang adalah ²³⁷Np dengan t½ sebesar 2,16 juta tahun, tidak ada apa-apanya jika dibanding usia tata surya.
Ketika radionuklida meluluh menjadi nuklida baru, terdapat beberapa pola yang akan selalu diikuti. Pola-pola ini berjumlah empat jenis dan diperlihatkan pada tabel berikut.
![]() Jenis-jenis deret peluluhan
Jenis-jenis deret peluluhan
Berdasarkan tabel tersebut, hal yang paling mudah dilihat perbedaannya adalah pada nomor massa. Untuk setiap pola atau deret (series) ada perbedaan nomor massa sebesar 1. Ini dikarenakan perubahan nomor massa hanya akan terjadi jika radionuklida meluluh dan memancarkan radiasi alpha. Ketika hal ini terjadi, radionuklida akan secara otomatis kehilangan dua buah proton dan dua buah neutronnya. Tetapi, ketika peluluhan yang terjadi adalah peluluhan yang memancarkan β atau γ, nomor massa tidak mungkin berubah.

Gambar diatas merupkan salah satu contoh peluluhan dari deret Thorium. ²³²Th menjadi radionuklida induk yang kemudia meluluh dan berubah menjadi raionuklida-radionuklida lain. Dari gambar diperlihatkan perubahan radionuklida dari satu jenis ke jenis yang lain dengan mengubah nilai nomor masa dan nomor atomnya. Radionuklida ini akan terus menerus bergerak untuk mendekati garis kestabilan agar bisa menjadi nuklida baru yang stabil.
Dari proses yang diperlihatkan diatas, bisa diperhatikan bahwa ²¹²Bi dapat berubah dengan dua cara yaitu menjadi ²⁰⁸Tl atau ²¹²Po. Kejadian semacam ini dinamakan dengan istilah branching atau percabangan, suatu kejadian dimana sebuah radionuklida dapat meluluh dengan lebih dari satu cara.

Peluluhan β+
Sama halnya dengan peluluhan β-, peluluhan β+ jug amenghasilkan partikel sampingan yaitu neutrino. Salah satu contoh peluluhan β+ adalah peluluhan yang terjadi pada ¹⁴O berdasarkan persamaan berikut.

Bukan hanya peluluhan β+ dan β- saja yang dapat menghasilkan produk sanmpingan berupa neutrino atau anti-neutrino. Ada juga reaksi yang dikenal sebagai electron capturing atau penangkapan elektron yang juga akan menghasilkan neutrino. Sama juga dengan peluluhan beta, neutrino nantinya akan membawa sebagian energi yang dihasilkan dari proses peluluhan.
Secara sederhana sebuah atom terdiri dari dua buah bagian utama, inti atom dan elektron. Elektron yang terdapat pada sebuah atom akan mengitari inti atom layaknya bumi dan planet-planet yang mengitari matahari (tentu dengan beberapa pengecualian karena elektron berperilaku berdasarkan hukum mekanika kuantum sedangkan planet-planet berdasarkan hukum mekanika Newton).
Karena elektron-elektron yang bermuatan negatif ini berputar mengitari inti atom yang bermuatan positif, maka akan ada kemungkinan dimana elektron jatuh ke dalam inti atom dna terjadi fenomena penangkapan elektron. Terlebih lagi jika jenis atomnya adalah atom non-logam dimana ada banyak elektron di dalam sebuah atom dan di saat yang bersamaan jari-jarinya berukuran kecil.
Elektron yang dapat jatuh ke dalam inti atom adalah elektron-elektron yang berada pada kulit K atau L, yaitu kulit orbit elektron yang paling dekat dengan inti atom. Reaksi yang terjadi pada proses penangkapan elektron dapat dituliskan sebagai berikut.

Prosesn ini akan menghasilkan neutrino, sama halnya dengan proses pemancaran radiasi β+ karena kedua proses ini adalah proses yang sama-sama melibatkan perubahan proton.
Peluluhan Gamma
Peluluhan gamma adalah satu-satunya jenis peluluhan yang tidak mengakibatkan perubahan nomor massa maupun nomor atom. Itu artinya, fenomena ini tidak membuat jumlah proton atau pun neutron beertambah seperti pada peluluhan alpha juga tidak mengakibatkan berubahnya proton menjadi neutron atau sebaliknya seperti peluluhan beta.
Peluluhan ini hanya terjadi pada inti atom yang kurang stabil. Biasanya terdapat proton atau neutron yang memiliki energi berlebih sehingga menyebabkan ketidakstabilan. Kondisi ini harus segera diubah yaitu dengan cara melepaskan energi yang berlebihan ini. Energi ini lalu dilepaskan dan dibawa dalam bentuk gelombang elektromagnetik atau foton ber-spektrum γ (gamma).
Reaksi dari peluluhan γ dapat dituliskan sebagai berikut.

Nuklida Radioaktif
Telah disepakati bersama bahwa semua partikel yang ada di alam semesta ini terbentuk dan bermula dari ledakan besar big bang yang terjadi 13,7 miliar tahun silam. Ketika ledakan ini terjadi, tidak serta merta membuat atom-atom berat langsung terbentuk. Ada proses panjang yang harus dilewati sampai akhirnya alam semesta kita menjadi alam semesta seperti yang kita ketahui sekarang.
Alam semesta hanya bisa menyediakan proton dan neutron bebas yang akhirnya bersatu dan membentuk atom-atom hidrogen, dimana atom-atom hidrogen ini menjadi penyusun utama dari semua jenis bintang. Ketika sebuah bintang sudah terbentuk, terjadilah pembakaran yang memicu terbentuknya nuklida-nuklida lain dengan massa yang lebih besar. Sampai akhirnya bintang sudah tidak mampu melakukan pembakaran lagi dan meledakkan supernovae atau planetary nebulae. Ketika ledakan ini terjadi, terbentuk lagilah nulida-nuklida yang lebih berat yang tidak mungkin dibentuk di dalam sebuah bintang.
Bumi yang kita tinggali sekarang mengandung beberapa unsur yang dibentuk dari semua proses panjang ini. Ada yang mengatakan bahwa semua unsur yang pernah terbentuk di alam semesta pasti bisa ditemukan di Bumi tapi sudah habis meluluh, tetapi ada juga yang mengatakan bahwa Bumi tidak mengandung semua unsur yang ada di alam semesta.
Tetapi ketika kita mempertimbangkan usia bumi saat ini, akan sangat sulit untuk membuktikan bahwa semua unsur pernah ada di Bumi. Usia Bumi dan Matahari bisa diperkirakan sama, yaitu sekitar 4,5 miliar tahun (sepertiga dari usia alam semesta). Dari jangka waktu yang selama ini, akan ada besar kemungkinan terdapat radionuklida yang telah meluluh total sehingga tidak mungkin ditemukan saat ini. Dari pengamatan dan penelitian yang telah dilakukan, tidak mungkin ada radionuklida di Bumi yang lebih berat dari 238U, kecuali jika radionuklida ini adalah radionuklida hasil proses buatan manusia. Salah satu radionuklida yang memiliki waktu-paro paling panjang adalah ²³⁷Np dengan t½ sebesar 2,16 juta tahun, tidak ada apa-apanya jika dibanding usia tata surya.
Ketika radionuklida meluluh menjadi nuklida baru, terdapat beberapa pola yang akan selalu diikuti. Pola-pola ini berjumlah empat jenis dan diperlihatkan pada tabel berikut.
Berdasarkan tabel tersebut, hal yang paling mudah dilihat perbedaannya adalah pada nomor massa. Untuk setiap pola atau deret (series) ada perbedaan nomor massa sebesar 1. Ini dikarenakan perubahan nomor massa hanya akan terjadi jika radionuklida meluluh dan memancarkan radiasi alpha. Ketika hal ini terjadi, radionuklida akan secara otomatis kehilangan dua buah proton dan dua buah neutronnya. Tetapi, ketika peluluhan yang terjadi adalah peluluhan yang memancarkan β atau γ, nomor massa tidak mungkin berubah.

Bentuk peluluhan dari deret thorium, satu dari empat jenis peluluhan yang ada
Gambar diatas merupkan salah satu contoh peluluhan dari deret Thorium. ²³²Th menjadi radionuklida induk yang kemudia meluluh dan berubah menjadi raionuklida-radionuklida lain. Dari gambar diperlihatkan perubahan radionuklida dari satu jenis ke jenis yang lain dengan mengubah nilai nomor masa dan nomor atomnya. Radionuklida ini akan terus menerus bergerak untuk mendekati garis kestabilan agar bisa menjadi nuklida baru yang stabil.
Dari proses yang diperlihatkan diatas, bisa diperhatikan bahwa ²¹²Bi dapat berubah dengan dua cara yaitu menjadi ²⁰⁸Tl atau ²¹²Po. Kejadian semacam ini dinamakan dengan istilah branching atau percabangan, suatu kejadian dimana sebuah radionuklida dapat meluluh dengan lebih dari satu cara.
